稀土除铊核心原理是:先氧化把 Tl⁺转为 Tl³⁺,再用沉淀 / 吸附 / 离子交换把铊从稀土浸出液里选择性分离,同时尽量不损失稀土。下面分原理、主流工艺与关键控制三部分讲清楚。
一、铊在稀土体系里的存在形态
稀土矿(尤其风化壳淋积型)酸浸后,铊主要以Tl⁺(一价)为主,少量Tl³⁺(三价):
- Tl⁺:性质像 K⁺/Na⁺,溶解度高、难直接沉淀,是除铊难点。
- Tl³⁺:性质像 Al³⁺/Fe³⁺,易水解、易沉淀,易去除。
- 稀土浸出液通常pH=1–4、硫酸 / 盐酸体系,Tl⁺稳定、Tl³⁺易还原,所以必须先氧化。
二、核心原理:氧化 + 分离两步
1. 氧化(把 Tl⁺→Tl³⁺,必备前置)
用强氧化剂在酸性条件下把一价铊氧化为三价铊,大幅提高后续去除效率:
- 常用:KMnO₄、H₂O₂、NaClO、O₃。
- 反应(以 KMnO₄为例):
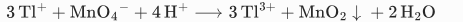
- 控制:pH=2–3、氧化剂过量 10–20%,避免稀土被氧化。
2. 分离(沉淀 / 吸附 / 离子交换,选择性除铊)
(1)化学沉淀法(主流,高浓铊首选)
- 硫化物沉淀(最常用):投加 Na₂S/NaHS,生成Tl₂S(Ksp≈10⁻²¹,极难溶):
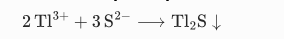
- 条件:pH=4.5–5.5(酸性防 H₂S 逸出,稀土不沉淀),去除率95–99%。
- 氢氧化物沉淀:调 pH=9–11,生成Tl(OH)₃(Ksp≈10⁻⁴⁴),但稀土也会沉淀,仅用于废水端。
- 铁盐 / 铝盐共沉淀:FeCl₃/Al₂(SO₄)₃生成胶体,吸附 Tl⁺/Tl³⁺,适合低浓铊(<1mg/L)。
(2)吸附法(深度除铊,低浓 < 20μg/L)
- 用改性活性炭、功能化树脂、分子筛,表面官能团(巯基、氨基)特异性吸附铊离子。
- 优势:pH=0–14 稳定、再生简单(盐酸 / 硫酸)、循环寿命 > 5 年,出水可稳定 < 2μg/L。
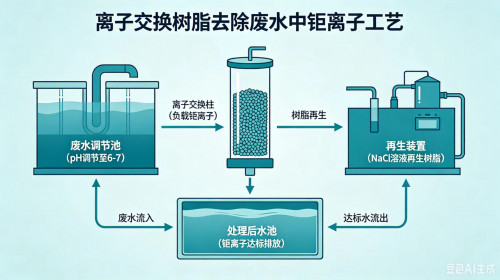
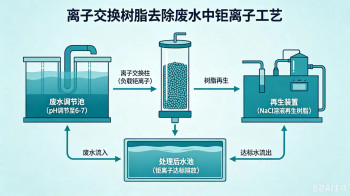
(3)离子交换法(精除,极低浓 ppb 级)
- 专用螯合树脂 / 阴离子交换树脂:酸性下 Tl³⁺与 Cl⁻形成TlCl₄⁻,被树脂交换吸附。
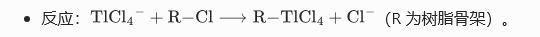












 官方公众号
官方公众号 官方小程序
官方小程序
发表用户评论,可得5积分,积分可兑换“100元天猫卡”等实物好礼;更有机会成为“星级评价官”,享受专属权益,快来积极参与吧!
共0条